Inklusionslegememyositis (IBM)
Inklusionslegeme myositis (IBM) er en muskelsygdom, der primært optræder hos personer over 50 år. Den er beskrevet som den muskelsygdom, der hyppigst debuterer efter 50-års alderen. Sygdommen kaldes også sporadisk IBM (s-IBM), da den næsten altid forekommer sporadisk, uden familiær ophobning (selvom der er beskrevet få tilfælde af familiær ophobning).
 Der findes også en lignende muskelsygdom der kaldes GNE-myopati (også kaldet hereditær inklusionslegememyopati (h-IBM)), som er arvelig og har en mutation i GNE-genet. Muskelpatologien for disse to lidelser er meget ens, men GNE-myopati har en anden patogenese (sygdomsudvikling) end s-IBM og et lidt andet sygdomsforløb (se kort beskrivelse af GNE-myopati under ”IBM for privatpersoner”).
Der findes også en lignende muskelsygdom der kaldes GNE-myopati (også kaldet hereditær inklusionslegememyopati (h-IBM)), som er arvelig og har en mutation i GNE-genet. Muskelpatologien for disse to lidelser er meget ens, men GNE-myopati har en anden patogenese (sygdomsudvikling) end s-IBM og et lidt andet sygdomsforløb (se kort beskrivelse af GNE-myopati under ”IBM for privatpersoner”).
Patogenesen for IBM er ikke helt klarlagt, men menes at involvere et samspil mellem inflammatoriske og degenerative processer. Der er ingen specifik farmakologisk behandling, der har vist sig effektiv.
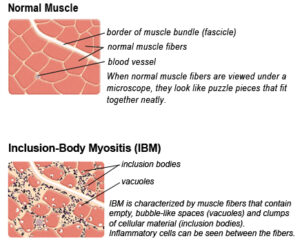 IBM har en karakteristisk klinisk fænotype og karakteristiske histopatologiske fund, og navnet inklusionslegeme refererer til den måde muskelcellerne ser ud i et mikroskop. Klinisk findes typisk svaghed af fingerfleksorer, knæekstensorer, anklens dosal fleksorer og dysfagi.
IBM har en karakteristisk klinisk fænotype og karakteristiske histopatologiske fund, og navnet inklusionslegeme refererer til den måde muskelcellerne ser ud i et mikroskop. Klinisk findes typisk svaghed af fingerfleksorer, knæekstensorer, anklens dosal fleksorer og dysfagi.
Selv om IBM normalt ikke påvirker levealderen, kan patienter få udtalt påvirkning af funktionsevnen ved fremskredne stadier af sygdommen.
-
IBM har en prævalens på ca. 3/100.000. Der lever ca. 150 personer med sygdommen i Danmark.
Både mænd og kvinder kan få sygdommen, men man regner med, at der er ca. 1½ gange så mange mænd som kvinder, der får sygdommen. Dette er modsat andre myositter, hvor der er en overvægt af kvinder.
-
Der er på nuværende tidspunkt ingen viden om, hvorfor nogen får sygdommen. IBM er i de fleste tilfælde en sporadisk lidelse.
Patogenesen for IBM er ikke helt klarlagt, men består sandsynligvis af et samspil mellem inflammatoriske og degenerative processer, men det er fortsat uklart, om den primære proces er immunmedieret eller degenerativ.
Inflammatorisk årsag
Tilstedeværelsen af inflammatoriske celler indikerer en inflammatorisk komponent i patogenesen. Cellerne er for det meste cytotoksiske T-celler (CD8+) og makrofager, der invaderer ikke-nekrotiske muskelfibre, og T celler (CD4+) og makrofager, der ligger omkring disse muskelceller. Aktiveringen af T-celler er sandsynligvis en antigen-drevet respons på baggrund af tilstedeværelsen af antigen præsenterende celler i muskelfibrene.
Derudover understøtter tilstedeværelsen af antistof rettet mod muskelproteinet cN1A en humoral komponent i patogenesen. Der er også tiltagende beviser for, at betændelse kan forårsage sekundære degenerative processer.
Degenerativ årsag
En degenerativ komponent i patogenesen understøttes bl.a. af tilstedeværelsen af vakuoler med proteininkluderinger, samt mitokondrie dysfunktion. Derudover underbygges en degenerativ årsag yderligere af, at der ikke er nogen synderlig effekt af immunmodulerende behandling.
Proteininkluderingerne i IBM indeholder en bred vifte af proteiner, som fx β-amyloid, der akkumuleres i muskelfibrene med en potentiel cytotoksisk effekt. Denne proteinakkumulering kan så teoretisk udløse en inflammatorisk reaktion.
Proteinakkumulering ses også ved andre neurodegenerative lidelser, fx ved sygdommen Alzheimers, hvor der findes den samme form for patogenetiske proteinakkumulering i hjernen, med fx β-amyloid der aflejres ekstracellulært. Selvom IBM og Alzheimers sygdom begge har β-amyloid aflejringer i henholdsvis musklerne og hjernen, er der dog ikke fundet en sammenhæng mellem disse to lidelser.
Der er altså ingen enkelt, velforstået teori til at forklare patogenesen ved IBM. Nogle muskelceller er påvirket af invaderende cytotoksiske T-celler, mens andre ikke har nogen åbenbar årsag til deres morfologiske abnormiteter, og er blevet kaldt degenerative.
-
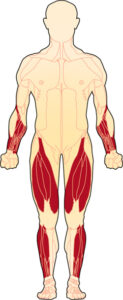
IBM har karakteristisk svaghed af fingerfleksorer, knæekstensorer og anklens dosalfleksorer samt dysfagi. Således er de kliniske kendetegn svaghed og atrofi af m. quadriceps og underarmens fleksorer. Mange oplever pludselige/sporadiske fald som de første symptomer. Med tiden kan andre muskelgrupper påvirkes, fx hals- og nakkemuskler, muskler i mave-brystkasse og dermed respirationen. Svaghed i de distale fingerfleksorer er ofte et af de tidligste fund. Der er ingen andre organmanifestationer
De karakteristiske kliniske træk ved IBM er følgende:
- Snigende debut: Sygdomsforløbet er langsomt progredierende. Der går gennemsnitlig 5 år fra de første symptomer viser sig, til diagnosen er stillet.
- Asymmetrisk og distal muskelinvolvering: Ved IBM påvirkes oftest håndledsmusklerne, fingerfleksorerne og fodekstensorerne
- Muskelatrofi: Atrofi og nedsat kraft af fingerfleksorerne, håndledsfleksorerne, og quadriceps, som forværres med progressionen af sygdommen.
- Dysfagi: ses hos ca. 30 % til 50 % af patienterne med IBM. Dysfagi kan medføre lungeinfektioner pga. aspiration. Læs mere om dysfagi
De første symptomer kan variere fra patient til patient. Det mest almindelige træk er en snigende debut og progressiv udvikling af muskelsvaghed, der typisk manifesterer sig som følgende:
- Vanskeligheder i forbindelse med trappegang eller ved at rejse sig fra en stol.
- Nedsat ganghastighed pga. svaghed over hoftefleksorerne.
- Hyppige fald på grund af, at knæene giver efter grundet svaghed af quadricepsmusklerne i lårene.
- Dropfod og dermed tendens til at snuble.
- Vanskeligheder med at rede håret og nå de øverste skabe grundet svaghed over skulderbælte.
- Nedsat grebsstyrke grundet svaghed af fingerfleksorerne.
Der er ikke noget, der tyder på, at IBM påvirker den forventede levetid. Men tab af gangfunktion, dysfagi og risikoen for aspirationspneumoni udgør nogle af de største komplikationer til sygdommen. Opgørelser viser, at tab af gangfunktion optræder hos ca. 1/3 efter 14 års sygdom, og hos næsten alle efter 20 års sygdom.
-
Der findes ingen kurativ behandling af IBM.
På trods af den inflammatoriske komponent ved IBM er effekten ofte fraværende, og i bedste fald mild og forbigående, af immunosuppressiv behandling (som kortikosteroider, intravenøs immunoglobulin (IVIG), methotrexat og azathioprine).
På grund af den manglende effekt af immunosuppression, er behandling rettet mod den degenerative proces blevet et nyt potentielt terapeutisk mål, og der forskes i at finde effektive lægemidler, der er målrettet den degenerative proces. Dog er der indtil videre ikke fundet lægemidler, der har vist sig effektive, ligeledes er der ingen data, der understøtter effekten og sikkerheden af stamcellebehandling ved IBM.
Dysfagi: Det er vigtigt både at forebygge aspirationspneumoni og sikre at personer med IBM for sufficient ernæring. Derfor anbefales det at involvere de kommunale ergoterapeuter mhp. dysfagiscreening og vejledning. Der kan være behov for løbende at konsistensregulerer, som sygdommen udvikler sig.
Ved svær dysfagi kan der i nogle tilfælde være behov for at anlægge ernæringssonde.
Fysioterapi og rehabilitering er et vigtigt aspekt af behandlingen. Motion og vedligeholdende træning betragtes som en meget vigtig del af behandlingen, og kan hjælpe med at forbedre muskelstyrken og forsinke svaghed og funktionsnedsættelse og dermed livskvaliteten for patienterne. Gradueret rehabilitering ved en erfaren fysioterapeut bør startes så hurtigt som muligt for at opnå de bedste resultater.
-
Det er vigtigt løbende at være opmærksom på, hvordan man kan opnå og vedligeholde færdigheder, og hvornår det kan være relevant at bruge hjælpemidler eller praktisk hjælp for at opnå en så stor selvstændighed som muligt.
For voksne gælder, at den nedsatte muskelkraft og øgede udtrætning kan medføre behov for ændring i arbejdslivet.
-
Medicin: Personer med muskelsvind kan reagere anderledes eller mere kraftigt på medicin. Det gælder særligt for nogle typer smertestillende medicin og visse bedøvelsesmidler. Det er derfor vigtigt altid at fortælle den læge, der ordinerer medicinen, om diagnosen. Særligt skal man være opmærksom på, om personen har hjerte- eller respirationspåvirkning udover sin muskelsvind. Hvis lægen er i tvivl, kan han eller hun kontakte børnelægen eller neurologen på det hospital, hvor personen går til kontrol.
RCFM har udarbejdet et vejledende akutkort, hvor der også er beskrevet særlige hensyn.
Forsikring: Diagnosen IBM vil i mange tilfælde kunne udløse forsikringssum ved kritisk sygdom, derfor anbefales det, at personer, der får stillet diagnosen, undersøger dette med sit forsikringsselskab
Mestring Det kan være en psykisk belastning at få at vide, at man har en muskelsvindsygdom. De mange nye og usikre situationer, der følger med, og det uforudsigelige fremtidsperspektiv kan skabe bekymring og usikkerhed.
Da IBM er en progredierende lidelse, skal personen løbende tilpasse sig og forholde sig til, at funktionsniveauet ændres, og at man ikke kan det samme som tidligere. Der kan naturligt komme nogle psykiske reaktioner på dette. Læs mere om det her
Referencer
Inclusion Body Myositis – StatPearls – NCBI Bookshelf (nih.gov)
Inclusion Body Myositis: Update on Pathogenesis and Treatment (nih.gov)
OMIM Entry – % 147421 – INCLUSION BODY MYOSITIS
Search of: Inclusion body myositis – List Results – ClinicalTrials.gov
Cardiac and Musculoskeletal Defects and Their Role in Common Alzheimer Disease Morbidity and Mortality (https://ajp.amjpathol.org/article/S0002-9440(20)30235-2/fulltext)
Sporadic inclusion-body myositis and hereditary inclusion-body myopathies: diseases of oxidative stress and aging? V Askanas (https://pubmed.ncbi.nlm.nih.gov/9678308/)
Familial inflammatory inclusion body myositis, B Ranque-Francois (https://pubmed.ncbi.nlm.nih.gov/15769920/)
Inclusion body myositis (Concept Id: C0238190) – MedGen – NCBI (nih.gov) (Indeholdende flere referencer til etiology, diagnosticering, patogenese, behandling etc.)