Forskning i medicin mod ALS
ALS er en meget kompliceret sygdom, og der er mange forskningsprojekter i gang, der prøver at blive klogere på sygdommen, udvikle ny medicin, eller undersøge eksisterende medicinske præparaters virkning på ALS.
Her kan du læse om forskningsprocessen og få tips til, hvor du kan finde mere viden om forskning om ALS.
Komplekse mekanismer og ukendte faktorer
Sygdomsmekanismerne i Amyotrofisk Lateral Sklerose (ALS) er uhyre komplekse, og på trods af intensiv forskning gennem mange år mangler de fleste brikker i puslespillet stadig. Der er dog bred enighed om, at der er tale om en sygdom af multifaktoriel karakter (dvs. at flere faktorer spiller en rolle i udviklingen af denne). Den aktuelle medicinske forskning er derfor præget af forsøg på at ramme forskellige dele af de sygdomsmekanismer, vi allerede kender, eller som man formoder har en betydning for sygdommens udvikling.
De senere år er forskere desuden begyndt at kigge nærmere på selve definitionen af ALS i erkendelse af forekomsten af de mange forskelligartede sygdomsforløb. Der bliver aktuelt i de internationale forskermiljøer diskuteret, hvorvidt det vil give mening at definere ALS i flere undertyper.
På baggrund af de mange ukendte faktorer, samt manglen på behandlingsmuligheder, har en stor del af forskningen til formål at undersøge allerede eksisterende (og dermed også godkendte) medicinske præparater (evt. i ny kombination, eller i andre doser), der oprindeligt er udviklet med andre sygdomme for øje, men hvor der teoretisk set også kunne være en gavnlig effekt på ALS.
Ved platformtestning kan flere stoffer testes hurtigere
De forskellige faser, et klinisk forsøg skal igennem, er en meget tidskrævende proces, og man er derfor, som et helt nyt tiltag, begyndt at anvende specielle studiedesigns, hvor man taler om platform testning. Det er et studiedesign som oprindeligt er udviklet til kræftforskning, men som man nu afprøver på ALS.
En af udfordringerne ved den traditionelle form for forsøg er bl.a., at man deler forsøgsdeltagerne op i to lige store grupper: en der får det aktive stof, og en der får placebo (ikke aktivt stof). Hvis der er flere forskere, der gerne vil have testet forskellige stoffer på ca. samme tidspunkt, kan det være svært at få deltagere nok, da ALS er en sjælden sygdom. Samtidig kan det afholde nogle fra at deltage, når der kun er 50% chance for at få det aktive stof.
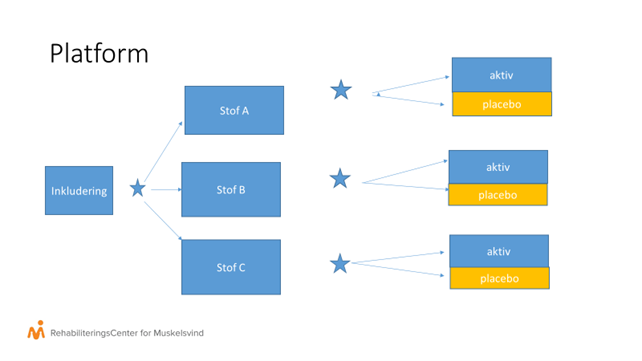
Ved platform testning er formålet at kunne teste flere stoffer samtidig, hurtigere og med færre i antal, der får placebo. Fremgangsmåden er:
- Inklusion af x antal forsøgsdeltagere, som bliver randomiseret (fordelt ved lodtrækning) til f.eks. 3 forskellige stoffer.
- De 3 lige store grupper randomniseres så igen, men denne gang i 1/3 og 2/3, hvor de 2/3 får det aktive stof.
- Når forsøget afsluttes, kan man samle de 3 placebogrupper og bruge dem som sammenligningsgrundlag for alle 3 stoffer.
Denne form for testning skal nu afprøves på ALS forskningen i The Healey ALS platform trail. Forsøget foregår i USA og er fordelt på 54 forskellige forsøgssteder.
Mange studier er i gang over hele verden
Over hele verden gennemføres der således mange forsøg og studier enten med det sigte at blive klogere på sygdommen, udvikle ny medicin, eller undersøge eksisterende medicinske præparaters virkning på ALS. Formålet er aktuelt at forsøge at sinke sygdommens progression (udvikling) og lindre følgesymptomerne, men det langsigtede formål er udvikling af en kurativ (helbredende) behandling.
På den amerikanske database Clinical Trials, som er et globalt register over anmeldte planlagte, igangværende, samt afsluttede studier, kan man holde sig orienteret omkring, hvilke studier der er i gang, samt hvilken fase de er nået til.
Oversigt over forsøg med behandlinger til ALS
Der er lige nu ca. 130 forsøg i gang, der tester medicin mod ALS på forskellige stadier. I det følgende kan du læse en kort beskrivelse af de forsøg, der er længst fremme.
-
PrimeC er en kombination af to allerede godkendte lægemidler (Ciprofloxacin, et Ibuprofen-lignende lægemiddel og Celecoxib, som er et antibiotikum). PrimeC retter sig mod tre faktorer, som menes at bidrage til ALS/MND:
- Betændelse i hjernen
- Unormal mikroRNA-aktivitet
- Ophobning af jern i nerveceller
Ved at reducere disse faktorer håber man at mindske skader på nerveceller og bremse sygdommens udvikling.
Forsøgsresultater
Et fase 2b-forsøg viste, at PrimeC er sikkert og godt tolereret. Der var tegn på langsommere sygdomsprogression og bedre lungefunktion hos behandlede patienter, men forskellene var ikke statistisk signifikante. En efterfølgende analyse peger dog på, at en undergruppe, der fulgte forsøgsprotokollen meget nøje havde signifikant effekt. Dette kræver yderligere forskning.Fase 3-forsøg
De amerikanske sundhedsmyndigheder (FDA) har netop givet grønt lys for opstart af et fase-3 forsøg. -
Tofersen er en type genterapi, der retter sig mod den arvelige form for ALS, hvor sygdommen sidder på SOD-1-genet. Medicinen benytter sig af såkaldte antisense oligonukleotider (ASO), som er i stand til at ’lukke ned for’ det gener, der er årsag til sygdommen.
Et fase 1-studie med deltagelse af 50 patienter Europa, USA og Canada viste gode resultater, bl.a. langsommere forværring af både funktioner, vejrtrækning og muskelstyrke.
På baggrund af de lovende resultater påbegyndte Biogen i foråret 2020 et fase 3-studie på 108 patienter. Studiet skulle vise om medicinen har same effekt på en større gruppe deltagere. De første resultater var ikke helt så lovende som forventet i forhold til at bremse sygdomsudviklingen. Forskerne undersøgte derfor, om der var større effekt, hvis behandlingen gives meget tidligt i forløbet. Dette forsøg viste at tofersen bremsede sygdomsudviklingen i forhold til vejrtrækning, styrke og livskvalitet.
Forsøget er afsluttet i juni 2024, og både det amerikanske og det europæiske medicinagentur, FDA og EMA har godkendt medicinen til markedsføring. Tofersen vil blive markedsført under navnet Qualsody, og skal gives som indsprøjtning i rygmarven.
I Danmark har Medicinrådet afslået, at Tofersen kan anvendes som et supplement til standardbehandlingen for ALS. Afslaget begrundes med, at de kliniske forsøg ikke har kunnet påvise en ændring i deltagernes funktionsniveau og at opfølgningstiden har været for kort. Derudover anfører Medicinrådet, at prisen er urimelig høj set i lyset af, at der ikke er en dokumenteret effekt.
Biogen tester lige nu tofersen i et separat fase-3 forsøg under navnet ATLAS. Dette forsøg adskiller sig fra de andre to forsøg idet medicinen testes på ca. 150 deltagere, som har den særlige SOD1 genmutation, men som endnu ikke har vist tegn eller symptomer på ALS. Forskerne vil med dette forsøg undersøge, om tofersen kan forsinke sygdomsdebut af ALS og/eller forhale nedgang i funktionsevnen, når symptomerne viser sig. Forsøget afsluttes i 2027.
-
Et hold israelske forskere udgav i oktober 2021 resultaterne af et forsøg med injektion af stamceller i patienter med ALS. Forsøget viser, at behandlingen var vel tolereret, og at den har potentiale til at forhale sygdomsudviklingen.
Stamcellerne, tages fra patienten selv, dyrkes i et laboratorium og bliver derefter leveret tilbage til patienten, enten som en indsprøjtning i blodbanen, i rygmarven eller i muskelvævet.
Stamcellerne er den type, der kaldes de mesenchymale stamceller, som er i stand til at danne knogle, brusk, fedt og andet bindevæv. Andre studier har også vist, at denne type stamceller kan forhale sygdomsudviklingen blandt patienter med ALS, men de har også vist, at effekten aftager med tiden.
Det israelske forskerhold ville derfor undersøge, om det var sikkert at give flere på hinanden følgende injektioner, og om man på den måde kunne opnå fornyet effekt.
Der blev ikke rapporteret om alvorlige bivirkninger. Hyppigste bivirkninger var hovedpine og ømhed omkring injektionsstedet lige efter behandlingen.
Af de 19 personer, der deltog i forsøget, oplevede 13, at sygdomsudviklingen blev forhalet med 25 %. Middelværdien for forhaling af sygdommen var 49 %, men der også var tre patienter, hvor forhalingen var mindre end 25 % og tre patienter, som ikke oplevede nogen effekt. Hos syv af patienterne sås endda en forbedring af funktionsniveauet.
De foreløbigt gode resultater giver grundlag for at gå videre med et større forsøg.
-
Masitinib er målrettet de celler i immunsystemet, som kaldes mastceller og makrofager. Andre studier har vist, at disse celler spiller en rolle i nedbrydningen af motorneuroner.
Fase 2- og 3-forsøg påviste en 27 % langsommere forværring af de fysiske funktioner ved 48 ugers måling med skalaen ALSFRS-R og en langsommere forværring af lungefunktionen. Producenten AB Science forsøgte af få medicinen godkendt i EU og Canada, men fik begge steder afslag. De blev i stedet rådet til at foretage et nyt fase 3-forsøg, som tilsyneladende endnu ikke er gået i gang.
(september 2025)
-
NurOwn er en stamcelleterapi, som anvender stamceller fra patienten selv. Formålet med behandlingen er, at få basisceller til at udvikle sig til nerveceller, eller celler der udskiller stoffer, som beskytter nerverne.
Et fase-2 forsøg viste en forbedring i funktionaliteten målt med ALSFRSr, og man indledte derfor et fase 3-forsøg på en større gruppe patienter.
Desværre viste resultaterne fra dette studie, som blev publiceret i november 2020, at behandlingen ikke havde nævneværdig virkning sammenlignet med placebo
Forskerne tilskrev dette, at man der i testgruppen var flere patienter med alvorlige forløb end i den tidligere testgruppe. I en gruppe med patienter I den tidlige fase af ALS, sås der nemlig stadig forskel på de patienter, der fik behandlingen, og dem, der fik placebo.
De amerikanske sundhedsmyndigheder mener imidlertid, at det lige så godt kan skyldes tilfældigheder, og at der derfor ikke på nuværende tidspunkt er grund til at ansøge om markedsføringstilladelse af medicinen.
Et opfølgende forsøg på patienter med tidlige og/eller moderate symptomer på ALS er planlagt, men endnu ikke gået i gang.
(September 2025)
-
AMX0035 er et præparat, som fremstilles af medicinalvirksomheden Amylyx. Formålet med medicinen er at forhindre, at neuronerne bliver uvirksomme eller dør. Virkningen er rettet mod mitokondrierne og det endoplasmatiske reticulum, som begge er strukturer, der findes inde i vores celler.
Godkendt i USA i 2022, men nu trukket tilbage.
Lægemidlet opnåede en forhåndsgodkendelse fra FDA i september 2022. Det skete på trods af, at FDA konkluderede, at der ikke var nok evidens til at afgøre, om lægemidlet kunne forlænge ALS-patienternes liv eller udskyde sygdomsprogression. Faktisk forelå der kun resultater fra et fase 2-studie.
Et stort opfølgende fase III-studie påviste ikke nogen signifikant effekt. I studiet fik 664 amerikanske patienter lægemidlet over en periode på 48 uger, men der blev ikke opnået en signifikant effekt i forhold til placebo. Derfor har Amylyx valgt at trække produktet tilbage fra markedet.
-
Medicinalvirksomheden Alexion, som er en del af AstraZeneca, annoncerede i august 2021, at de stopper fase 3-forsøget med Ravulizumab, da præparatet ikke har vist den ønskede effekt.
Ravulizumab er et antistof, der nedsætter aktiviteten i en del af immunforsvaret, og der har været en forventning om, at det kan bremse sygdomsudviklingen ved ALS.
Fase 3-forsøget blev udført på i alt 354 patienter med ALS, 73 forskellige steder på verdensplan.
I Danmark deltog Aarhus og Aalborg Universitetshospitaler samt Bispebjerg Hospital i forsøget.
-
Det danske medicinalfirma Orphazyme meddelte i maj 2021, at de stoppede forsøget med arimoclomol til patienter med ALS. Grunden til dette var, at resultaterne ikke viste de forbedringer, man havde håbet på.
Hvad man håbede på
Forventningen var, at arimoclomol ville få kroppens celler til selv at producere såkaldte heat shock-proteiner.
Heat shock-proteiner kan hjælpe cellen med at overkomme den stress, som den påvirkes af i forbindelse med udvikling af visse sygdomme, hvor proteiner ikke fungerer, som de skal, og klumper sig sammen til giftige aggregater.
Forskningshistorik
Et fase 3 forsøg på ALS-patienter blev opstartet i august 2018.
Medicinen fik fast track-godkendelse af de amerikanske sundhedsmyndigheder (FDA). Der blev ansøgt om godkendelse af medicinen hos de europæiske sundhedsmyndigheder i november 2020.
Forstudier viste en langsommere forværring af sygdommen i nogle målinger og dermed mulighed for længere overlevelse.
Selv om Orphazyme er en dansk virksomhed, har der ikke været danske deltagere med i forsøgene.
Hvordan bliver hospitaler godkendt til at deltage i forsøg?
For at et sygehus eller en afdeling kan deltage i forsøg med afprøvning af ny medicin, er der forskellige krav, de skal leve op til. For at blive godkendt til at kunne medvirke i afprøvning af ny medicin, kræver det dels godkendelse af lokale forhold fra medicinalfirmaets side, samt en national godkendelse til at få lov at indgå i det pågældende forsøg. I Danmark er det Lægemiddelstyrelsen og Videnskabsetiks komité, der står for godkendelsen af forsøget ved at vurdere undersøgelsens kvalitet, patientsikkerheden og etiske aspekter.
Begge dele (både medicinalfirmaets vurdering af lokale forhold og den nationale godkendelse) er ofte langsommelige og kan også være forbundet med en del omkostninger for medicinalfirmaet. Medicinalfirmaer vil derfor være interesseret i at blive godkendt i områder, hvor der er potentielt mange deltagere i forsøgene.
På trods af Danmarks lille størrelse globalt set har vi den fordel, at vi har et velfungerende sundhedsvæsen, og via vores registersystemer har vi stor viden om vore borgere og i dette tilfælde ALS-patienter. Størrelsen af vores population er dog klart en stor udfordring i forhold til at få medicinalfirmaerne til at være interesserede i at inkludere danske sites i deres studier. De danske neurologer arbejder løbende på at få lov at deltage i relevante studier.
Det godkendte lægemiddel har begrænset effekt
I Europa er der på nuværende tidspunkt kun et lægemiddel godkendt til behandling af ALS. Det er Riluzol (Rilutex®,Glentek®) som har en veldokumenteret, men desværre begrænset effekt. I bedste fald medfører behandling med Riluzol en forøget levetid på 2-3 måneder.
Undersøgelser har vist, at den gennemsnitlige overlevelsestid for de patienter, der fik Riluzol, var signifikant længere end for dem, der fik placebo. Ved sammenlignelige undersøgelser over 18 måneder finder man, at de patienter, der fik 100 mg Riluzol dagligt, overlevede i gennemsnit ca. 2 måneder længere end dem, der fik placebo. 50 mg Riluzol dagligt var ikke mere effektivt end placebo, og 200 mg dagligt var ikke mere effektivt end 100 mg dagligt. I de sene stadier af ALS virkede lægemidlet ikke bedre end placebo.
Kilde
https://www.ema.europa.eu/en/documents/overview/rilutek-epar-summary-public_da.pdf
En faglig gennemgang af alternative behandlingsmuligheder
I 2009 blev hjemmesiden www.alsuntangled.com oprettet af en amerikansk neurolog i erkendelse af manglen på uvildig rådgivning ift. alternative/ ikke lægeordinerede behandlinger af ALS. Som en naturlig konsekvens af at have fået en uhelbredelig diagnose vil mange selv opsøge viden om mulige alternativer til konventionel behandling.
Det kan være uhyre vanskeligt at gennemskue validiteten af de forskellige udsagn og anbefalinger, der findes på nettet. www.alsuntangled.com er en fagligt velfunderet og seriøs hjemmeside uden økonomiske incitamenter. På denne hjemmeside kan man holde sig orienteret om forskellige ”alternative” behandlingsmuligheder, som vil blive gennemgået med en videnskabelig tilgang, dvs. en vurdering og gennemgang af den viden, der aktuelt findes om et bestemt stof eller behandling f.eks. vitamin D eller akupunktur. Der er også mulighed for på hjemmesiden at have medindflydelse på, hvilke behandlinger der fremadrettet skal kigges på.